乳腺癌严重威胁女性健康,尤其是三阴性乳腺癌,由于缺作用靶点,化疗药物的总体疗效较差,加上传统药物载体难以同时实现长效血液循环和肿瘤深层给药,导致三阴性乳腺癌的治疗困难重重。因此,如何实现药物的深层渗透是治疗三阴性乳腺癌的关键科学问题。
针对该问题,太阳成集团杜建忠/范震团队构建了一种新型超声响应型多肽纳米凝胶,以平衡长效血液循环和肿瘤深层渗透的矛盾需求,具体研究思路如图1所示。
首先将能够靶向三阴性乳腺癌的 ICAM-1 抗体接枝于聚赖氨酸,并与Pluronic F127共组装,然后加入京尼平(Genipin)来交联聚赖氨酸,最终形成稳定的纳米凝胶。该凝胶能够在血液中长期保持稳定,实现长效循环。通过在病灶部位施加超声,促进Pluronic F127从纳米凝胶脱落,使得该纳米凝胶获得更优的形变性能,其杨氏模量从 336.78降低到 3.93 kPa,从而实现肿瘤深层渗透。
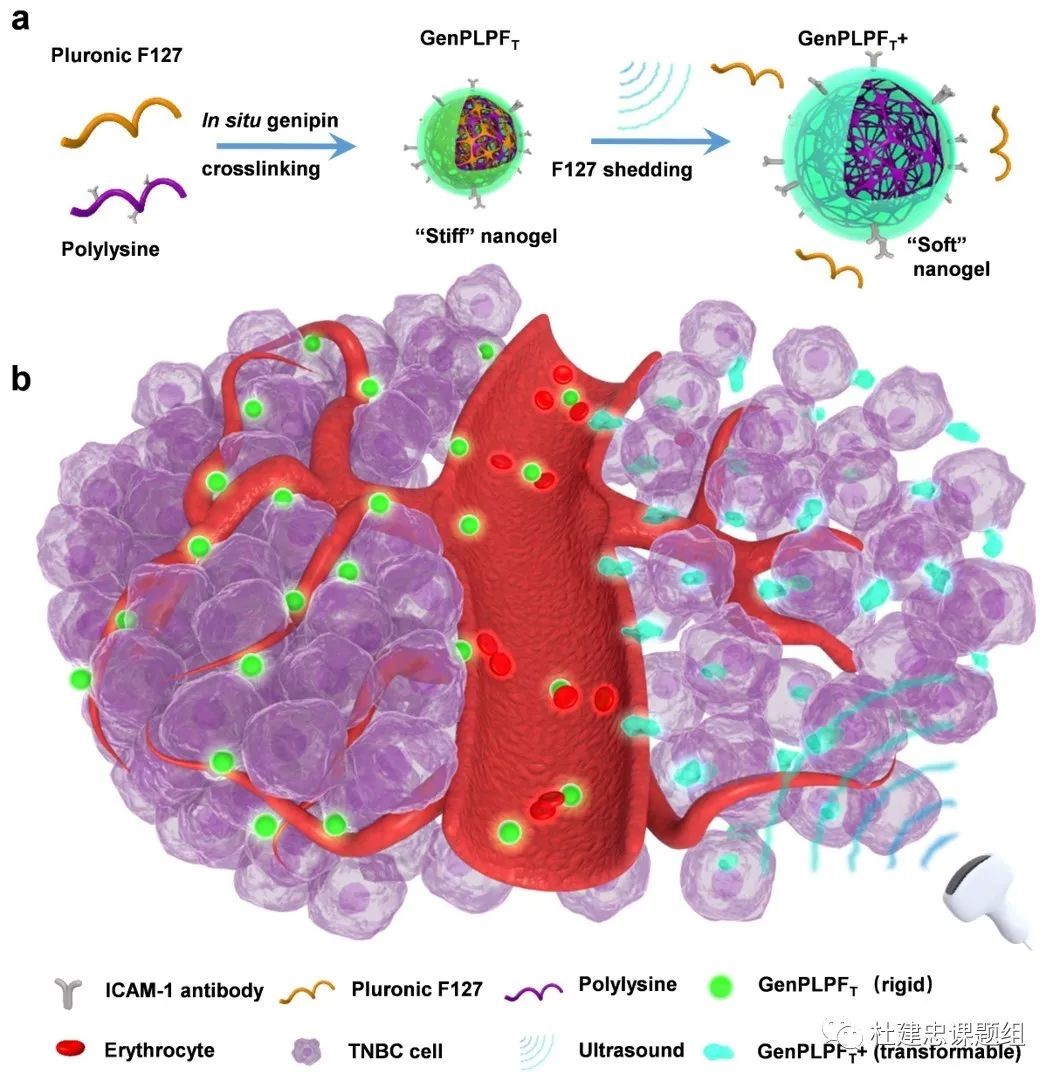
图1:声致变形多肽纳米凝胶用于深层肿瘤治疗。纳米凝胶可在血液中稳定存在,实现长效血液循环;在病灶部位施加超声即可导致纳米凝胶变形,从而实现针对三阴性乳腺癌肿瘤的深层渗透和有效治疗。
如图2所示,体外模拟三阴性乳腺癌实体瘤模型表明,该纳米凝胶能在超声作用下实现更好的肿瘤深层渗透和抑制效果。小鼠静脉注射后,相对刚性的纳米凝胶能通过主动靶向和长效血液循环实现在肿瘤部位高水平的富集。而在超声处理下,肿瘤部位的纳米凝胶变得更加柔软,通过形变增强实现肿瘤深层穿透,最终达到低水平的系统毒性和更高水平的抗耐药性肿瘤效果。
综上,这种声致变形凝胶能够同时实现长效血液循环和肿瘤深层药物递送,为肿瘤深层给药和三阴性乳腺癌治疗提供了新思路。
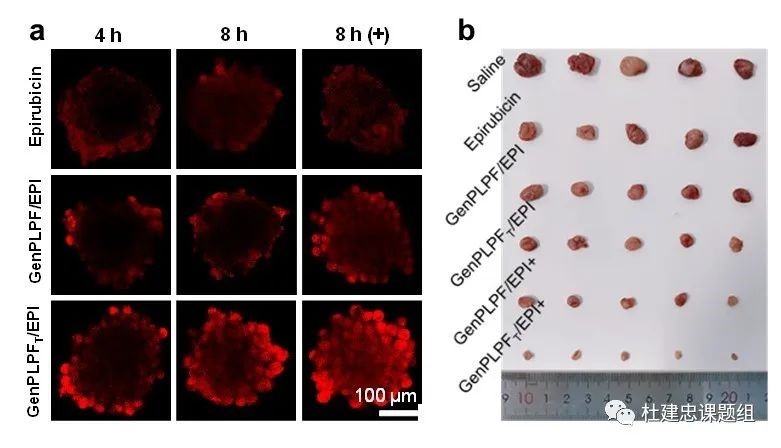
图2:(a)体外三阴性乳腺癌模型模拟多肽纳米凝胶的渗透性能;(b)体内抗肿瘤效果。
研究成果近期以“Ultrasound-Responsive Peptide Nanogels to Balance Conflicting Requirements for Deep Tumor Penetration and Prolonged Blood Circulation”为题发表在《美国化学学会·纳米》(ACS Nano 2022, DOI: 10.1021/acsnano.2c01407(点击可阅读全文))。太阳成集团高分子材料系博士生孙敏为论文的第一作者,太阳成集团杜建忠教授和范震研究员及以色列特拉维夫大学的Ehud Gazit教授为共同通讯作者。该研究得到了国家杰出青年科学基金(21925505)、国家自然科学基金面上项目(22075212)等资助。
